1. Введение. Значение витамина витамин D3 в физиологии и патологии человека
Витамин D3 (холекальциферол) — жирорастворимый прогормон, играющий критическую роль в поддержании гомеостаза организма. Главная функция витамина D3 - регуляция обмена кальция и фосфора, но, кроме этого, D3 регулирует иммунный статус, процессы в миокарде и нервной системе. Ниже представлен детальный анализ ключевых свойств витамина D3.
1.1. Метаболизм витамина D3
Витамин D3 синтезируется в коже под действием УФ-В излучения (290–315 нм) из 7-дегидрохолестерина или поступает с пищей и усваивается в кишечнике. Далее D3 гидроксилируется в печени до 25(OH)D3 (кальцидиол), а затем в почках — до активной формы 1,25(OH)₂D3 (кальцитриол) под контролем паратиреоидного гормона, кальция и фосфора [1].
1.2. Ключевые физиологические функции
Витамин D3 обеспечивает регуляцию кальций-фосфорного обмена, а следовательно - метаболизм костной ткани. В частности, кальцитриол индуцирует синтез кальций-связывающих белков (калбиндинов) в энтероцитах, обеспечивая всасывание 30–40% пищевого кальция и 60–80% фосфора [1]. Витамин D стимулирует дифференцировку остеокластов и поддерживает баланс между резорбцией и формированием костной ткани. Таким образом, витамин D3 управляет минерализацией костей. Дефицит витамина D3 приводит к рахиту у детей и остеомаляции/остеопорозу у взрослых [1]. Витамин D и его производные необходимы для нормального функционирования иммунной системы [2]. В частности, кальцитриол усиливает экспрессию антимикробных пептидов (кателицидинов) а также подавляет гиперреактивность Т-лимфоцитов, снижая риск аутоиммунных заболеваний. Витамин D ингибирует ренин-ангиотензиновую систему, снижая артериальное давление и риск развития гипертонической болезни [3]. Кальцитриол регулирует синтез нейротрофинов и защищает от нейродегенерации, таким образом, витамин D помогает сохранить когнитивные функции. Доказано, что низкий уровень D3 ассоциирован с депрессией и когнитивными нарушениями у пожилых [4]. Витамин D3 индуцирует апоптоз опухолевых клеток и подавляет ангиогенез в опухолях.
1.3. Возрастные изменения синтеза
После 20 лет концентрация синтезируемого в коже 7-дегидрохолестерина падает на ~13% каждые 10 лет. К 70 годам синтез витамина D3 уменьшается в 4 раза по сравнению с 20-летним возрастом [5]. Таким образом, люди старше 70 лет становятся группой риска по дефициту D3. Главными причинами снижения синтеза витамина D являются: 1) атрофия кожи и уменьшение площади синтеза провитамина D; 2) снижение почечной гидроксилазной активности (на 50% к 70 годам), что нарушает конверсию 25(OH)D3 в активный кальцитриол; 3) уменьшается выработка желчных кислот, что снижает усвоение витамина D на 20–40% [6]; 4) малоподвижный образ жизни и недостаток солнечного облучения [7].
1.4. Особенности синтеза витамина D в зависимости от географического положения
Синтез витамина D в коже напрямую зависит от угла падения УФ-В лучей (290–315 нм), который меняется в зависимости от сезона и широты. В частности, в умеренных широтах (40-50°, Смоленск, Москва, Нижний Новгород, Казань, Новосибирск и т.д.) синтез витамина D летом практически не происходит с ноября по февраль. На широтах около 60° (Санкт-Петербург) «зимний дефицит» длится до 6 месяцев [1]. У 40% жителей Канады, живущих на широтах 45–60°, уровень витамина D3 зимой снижается до концентрации в сыворотке крови < 20 нг/мл, что значительно ниже нормы и является критерием гиповитаминоза.
1.5. Нарушение усвоения витамина D3 из пищи
Усвоение витамина D3 из пищи реализуется благодаря сложным процессам, которые должны включать: 1) содержание жиров (липидов) в пище, обезжиренная диета снижает усвоение витамина D на 30–50% [8]; 2) нормальный уровень выработки желчных кислот, которые необходимы для образования необходимой для всасывания мицеллярной формы витамина D, у пожилых людей уменьшается выработка желчи, что снижает усвоение витамина D на 20–40% [6].
Ожирение является состоянием, которое снижает поступление витамина D в кости, нервную и мышечную ткани. Витамин D3 депонируется в жировой ткани, делая его недоступным для транспорта в другие ткани. Людям с ожирением требуются дозы витамина D, которые на 30–40% превосходят дозы для людей без ожирения [9]. Практически все виды патологии, затрагивающие желудочно-кишечный тракт, негативно влияют на усвоение витамина D. Из этого следует важный вывод о том, что оптимальная коррекция недостаточности витамина D3 возможна только на основе препаратов с повышенной биодоступностью, включая мицеллярные и липосомальные формы.
1.6. Патология, связанная с дефицитом витамина D
Самая распространенная патология, ассоциированная с дефицитом витамина D, это остеопороз, который является системным заболеванием скелета. Остеопороз характеризуется снижением костной массы и нарушением микроархитектоники костной ткани, что повышает риск переломов. У женщин, особенно в постменопаузе, остеопороз встречается в 4 раза чаще, чем у мужчин, из-за гормональных изменений (снижение эстрогена) и возрастного снижения абсорбции кальция. Витамин D3 играет центральную роль в патогенезе и профилактике этого заболевания. В норме кальцитриол (1,25(OH)₂D3) стимулирует синтез кальций-связывающих белков (калбиндин-D9k) в кишечнике, обеспечивая всасывание 30-40% пищевого кальция. При дефиците витамина D3 абсорбция снижается на 85-90%, что запускает компенсаторное повышение паратиреоидного гормона и деградацию костной ткани. Вторичный гиперпаратиреоз при дефиците D3 усиливает активность остеокластов, ускоряя потерю костной массы. Это особенно критично для женщин в постменопаузе, у которых естественная потеря костной ткани достигает 2-3% в год [10]. Кроме этого, витамин D3 регулирует концентрацию кальция и фосфора в крови, необходимых для гидроксиапатита — основного минерального компонента костей. При дефиците D3 возникает остеомаляция (размягчение костей), которая усугубляет остеопороз [11].
Витамин D3 поддерживает силу и координацию мышц через рецепторы VDR на миоцитах. Дефицит витамина D приводит к преждевременной дистрофии (дряхлению) мышц и их слабости. Сниженный тонус внутрикожных мышечных волокон ускоряет старение кожи. Слабость мышц (миопатия) увеличивает риск падений, что критично для женщин с остеопорозом, у которых даже незначительная травма может приводить к переломам длинных костей, включая шейку бедра, или позвонков.
Клинические наблюдения подтверждают прямую связь между дефицитом витамина D и остеопорозом: у женщин с уровнем D3 в сыворотке крови < 20 нг/мл риск переломов бедра на 30% выше, чем при уровне >30 нг/мл [7]. Женщины в постменопаузе с потреблением < 100 МЕ витамина D3 в сутки имели на 27% выше риск переломов по сравнению с теми, кто потреблял >600 МЕ витамина D в сутки [7].
1.7. Пути борьбы с дефицитом витамина D3
Так как дефицит витамина D3 приводит к развитию угрожающих патологических состояний, его профилактика и коррекция требует серьезных комплексных мероприятий. Основными принципами профилактики и терапии D3-дефицита являются: 1) индивидуальный подход, учитывающий возраст, географию проживания, особенности диеты и сопутствующую патологию пациентов; 2) мониторирование уровня D3 в сыворотке крови среди людей, относящихся к группам риска по недостаточности D3; 3) проведение профилактической инсоляции и периодический пероральный профилактический прием витамина D3; 4) проведение научных исследований, направленных на масштабный мониторинг недостаточности витамина D3 и на оценку эффективности препаратов, которые содержат витамин D3; 5) разработка новых D3-содержащих препаратов с повышенной биодоступностью.
Главным средством коррекции D3-дефицита следует считать препараты для перорального приема витамина D3 с повышенной биодоступностью, включая мицеллярные и липосомальные формы.
2. Цель исследования
Цель исследования - лабораторная оценка эффективности препарата «Super Osteo Complex» (производитель - ООО "Мицеллайн"), являющегося мицеллярной формой витамина D3 (холекальциферол).
3. Методология проведения исследования
Всего было обследовано 89 человек. Критериями включения в исследование были: 1) субъективные или объективные (клинические, лабораторные) признаки гиповитаминоза D3, и 2) прием препарата мицеллярного витамина D3 в течение срока от 25 до 60 дней непрерывно. Критериями исключения из исследования были: 1) возраст менее 16 лет, 2) нарушение сроков и правил приема мицеллярного витамина D3. В качестве источника витамина D3 применяли мицеллярную форму препарата «Super Osteo Complex» (производство ООО "Мицеллайн") [https://micelline.ru/product/super_osteo_complex], которую применяли перорально по 1 мл ежедневно. Концентрация основного вещества (холекальциферол) в препарате составляла 12500 МЕ в 1 мл.
Концентрация витамина D3 измерялась методом электрохемилюминесцентного иммуноанализа в сыворотке крови и выражалась в нг/мл. Нижним значением референсного интервала считали 30,0 нг/мл в соответствии с существующими рекомендациями [12].
4. Результаты.
4.1. Общая характеристика группы обследованных
Конкретные характеристики выборки пациентов суммированы в Таблице 1. Из 89 обследованных человек мужчины составляли 17,9%, женщины - 82,1%. Средний возраст мужчин (медиана) составлял 45 лет, средний возраст женщин (медиана) - 58 лет. Группа обследованных женщин была условно разделена на три подгруппы в соответствии с возрастным критерием. Количество женщин в младшей возрастной группе (≤45 лет) составляло 25 человек, в средней возрастной группе (от 46 до 60 лет включительно) было 22 человека, в старшей (>60 лет) - 26 человек.
4.2. Концентрации витамина D3 в сыворотке крови до приема препарата «Super Osteo Complex»
Концентрации витамина D3 сыворотке крови до приема препарата «Super Osteo Complex» в различных группах обследованных пациентов детально представлена в Таблице 2. В общей группе, включающей мужчины и женщины всех возрастов (n = 89), медиана концентрации витамина D3 в сыворотке крови составляла 29,20 нг/мл, что было ниже минимального референсного значения. Было установлено, что у 53,9% обследованных лиц наблюдалсь снижение концентрации витамина D3 в сыворотке крови ниже референсного уровня 30 нг/мл.
Таблица 1. Общая характеристика выборки обследованных
| № | Критерий | Количественный показатель |
|---|---|---|
| 1 | Общее количество | 89 |
| 2 | Мужчины, количество | 16 из 89 (17,9%) |
| 3 | Женщины, количество | 73 из 89 (82,1%) |
| 4 | Возраст общей группы, диапазон | от 16 до 86 лет |
| 5 | Средний возраст общей группы, медиана | 56 лет |
| 6 | Возраст группы мужчин, диапазон | от 19 до 86 лет |
| 7 | Средний возраст мужчин, медиана | 45 лет |
| 8 | Возраст группы женщин, диапазон | от 16 до 81 года |
| 9 | Средний возраст женщин, медиана | 58 лет |
| 10 | Младшая возрастная группа женщин ( ≤45 лет), количество | 25 |
| 11 | Средняя возрастная группа женщин (от 46 до 60 лет), количество | 22 |
| 12 | Старшая возрастная группа женщин ( >60 лет), количество | 26 |
| 13 | Критерии включения в исследование: 1) субъективные или объективные (клинические, лабораторные) признаки гиповитаминоза D3, и 2) прием препарата мицеллярного витамина D3 в течение срока от 25 до 60 дней непрерывно | |
| 14 | Критерии исключения из исследования: 1) возраст менее 16 лет, 2) нарушение сроков и правил приема мицеллярного витамина D3. | |
У женщин всех возрастов медиана концентрации витамина D3 составляла 29,30 нг/мл, у 52,1% женщин концентрация витамина D3 была ниже нормы. При сравнении концентрации витамина D3 среди женщин различных возрастных групп было установлено, что наименьшее количество женщин со снижением витамина D3 было в возрастной группе до 45 лет включительно и составляло 44% при медиане 33,70 нг/мл. В других возрастных группах процент женщин со сниженной концентрацией витамина D3 был значительно выше и колебался в пределах 53,8 - 59,1%, но существенно не различался (р >0,05) между возрастными группами 46-60 лет (медиана 29,25 нг/мл) и старше 60 лет (медиана 28,06 нг/мл). В группе мужчин 62,5% обследованных пациентов демонстрировали снижение уровня концентрация витамина D3 ниже референсного уровня при медиане 27,04 нг/мл.
Таблица 2. Концентрации витамина D3 сыворотке крови до приема препарата «Super Osteo Complex» (ООО "Мицеллайн")
| № | Группа | Кол-во человек, n | Количество человек с недостаточностью витамина D3 < 30 ng/ml, n (%) | .Средний уровень витамина D3 в сыворотке крови, медиана, Me (0,25%; 0,75%), нг/мл |
|---|---|---|---|---|
| 1 | Общая группа, мужчины и женщины всех возрастов | 89 | 48 (53,9%) | 29,20 (21,80; 39,10) |
| 2 | Женщины всех возрастов | 73 | 38 (52,1%) | 29,30 (21,69; 42,70) |
| 3 | Женщины до 45 лет включительно | 25 | 11 (44%) | 33,70 (24,80; 52,00) |
| 4 | Женщины 46 - 60 лет | 22 | 13 (59,1%) | 29,25 (22,80; 38,20) |
| 5 | Женщины старше 60 лет | 26 | 14 (53,8%) | 28,06 (17,69; 34,20) |
| 6 | Мужчины | 16 | 10 (62,5%) | 27,04 (22,25; 34,35) |
4.3. Содержание витамина D3 в сыворотке крови после курсового приема препарата «Super Osteo Complex»
Нежелательных побочных эффектов во время применения препарата «Super Osteo Complex» не наблюдалось.
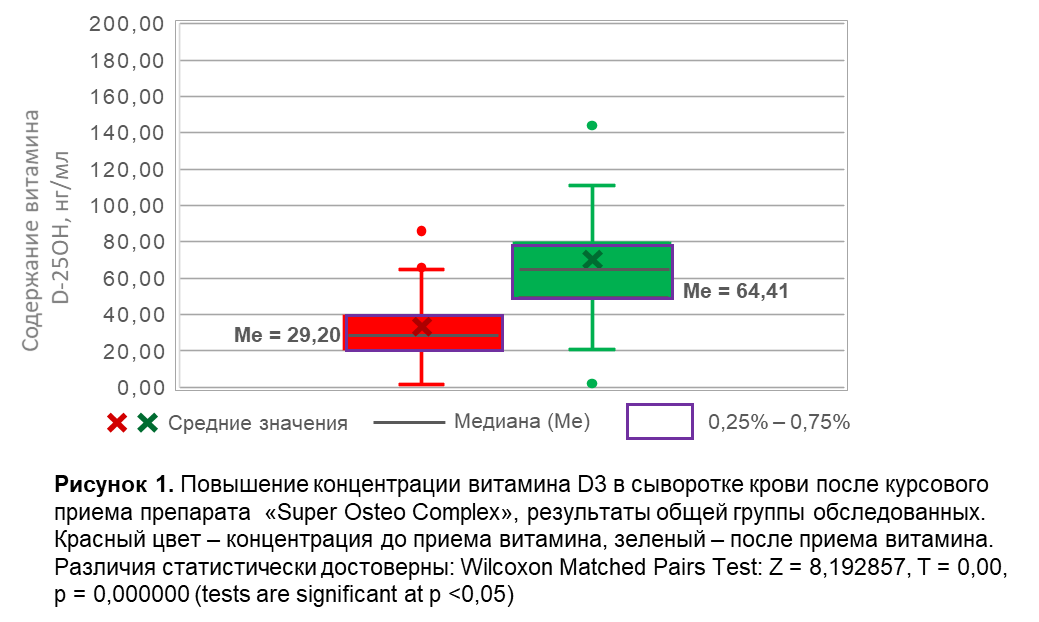
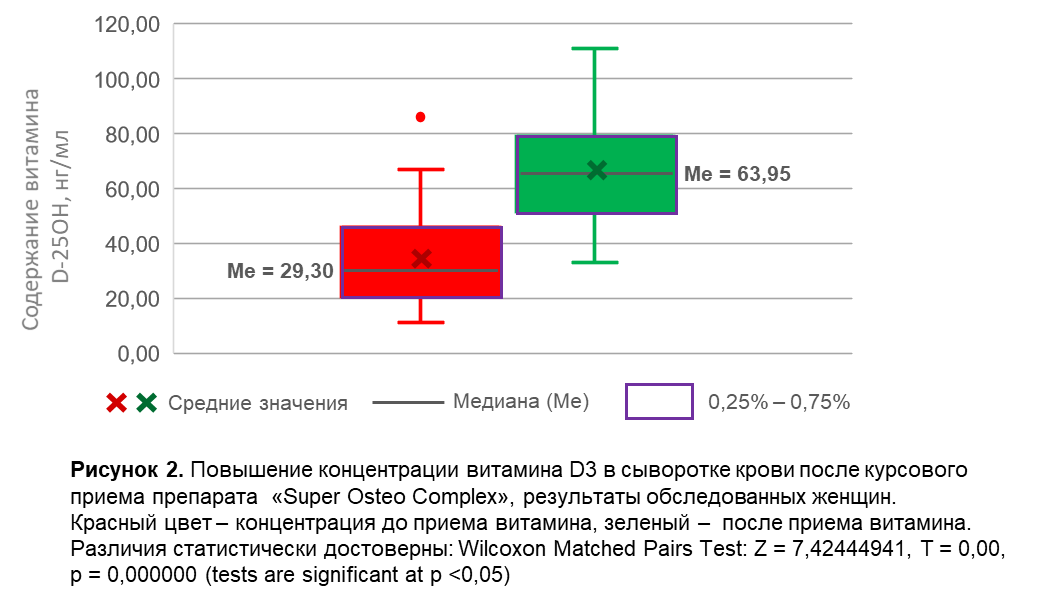
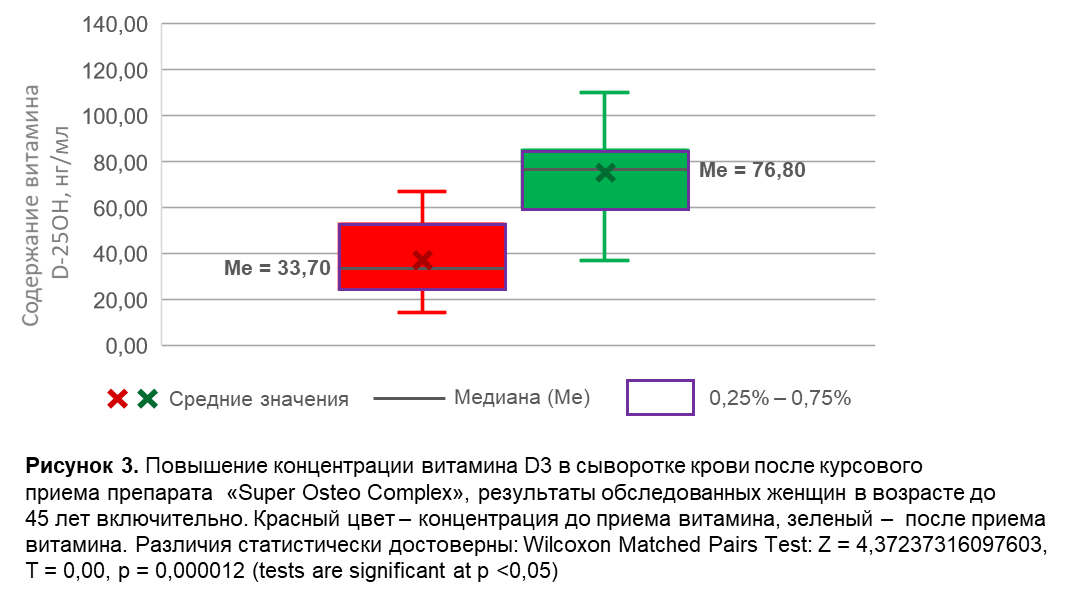
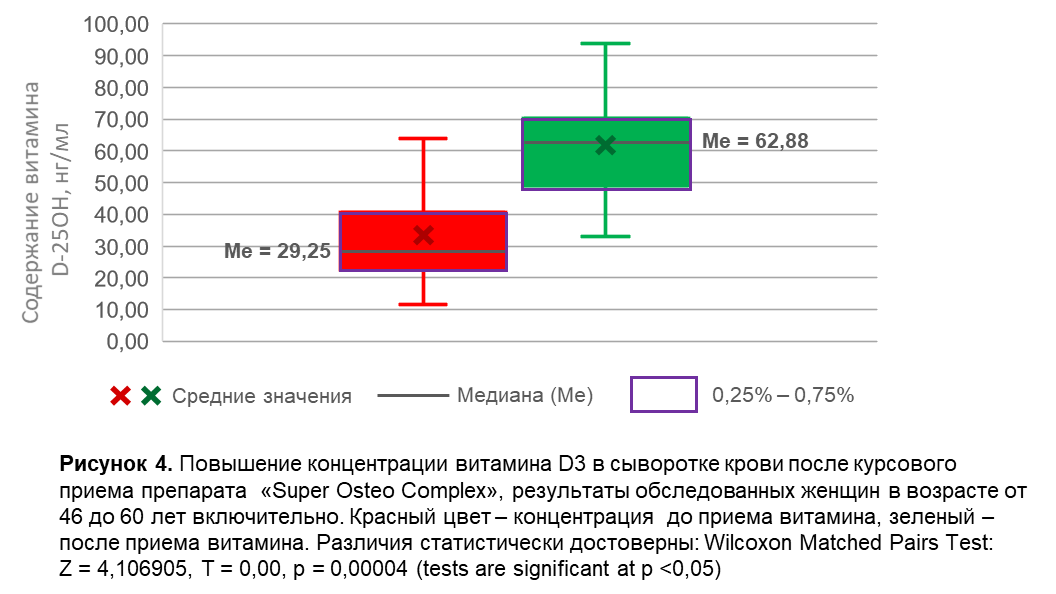
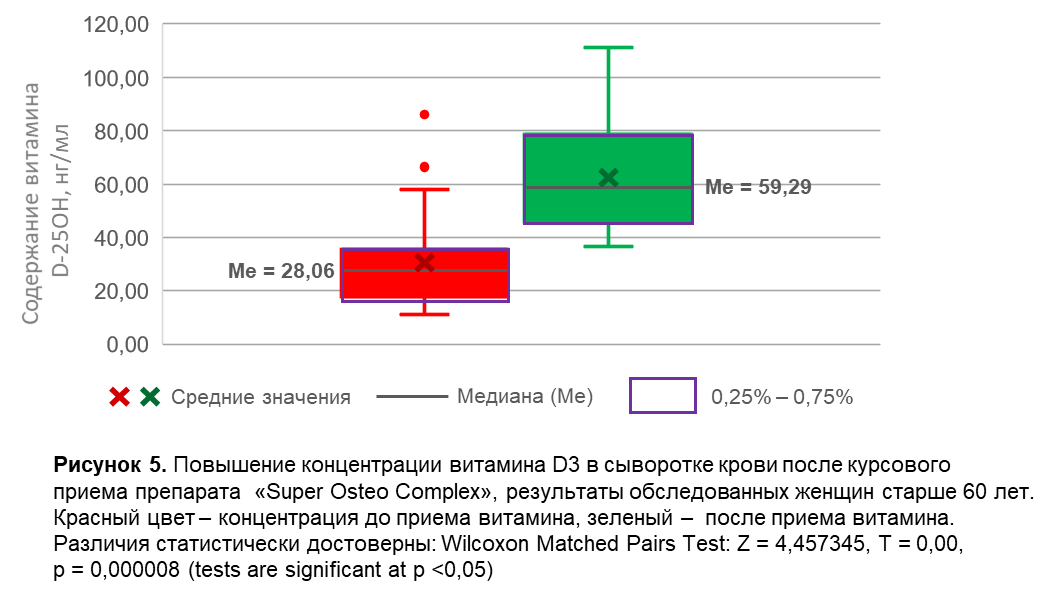
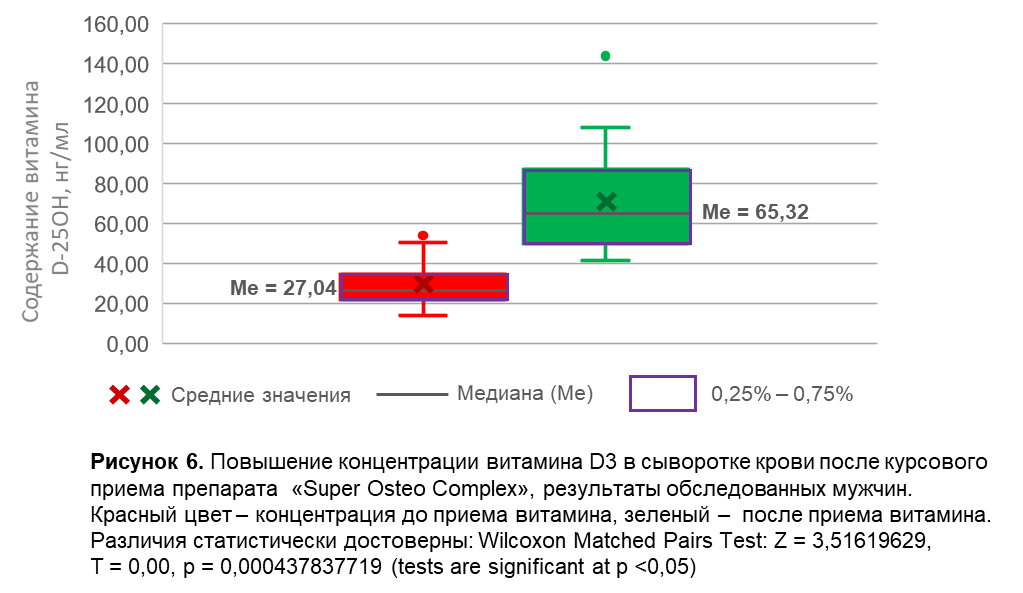
Динамика изменения содержания витамина D3 в сыворотке крови представлена на Рисунках 1 - 6. В общей группе, включающей мужчины и женщины всех возрастов (n = 89), медиана концентрации витамина D3 в сыворотке крови после курсового приема препарата составила 64,41 нг/мл, что было в 2,21 раза выше по сравнению с концентрацией до приема препарата (Рисунок 1). У женщин всех возрастов после приема препарата медиана концентрации витамина D3 составила 63,95 нг/мл, повышение в 2,18 раз (Рисунок 2). У женщин в возрастной группе до 45 лет включительно возрастов после приема препарата медиана концентрации витамина D3 составила 76,8 нг/мл, повышение в 2,28 раз (Рисунок 3). У женщин в возрастной группе от 46 до 60 лет включительно после приема препарата медиана концентрации витамина D3 составила 62,88 нг/мл, повышение в 2,15 раз (Рисунок 4). У женщин в возрастной группе старше 60 лет после приема препарата медиана концентрации витамина D3 составила 59,29 нг/мл, повышение в 2,11 раз (Рисунок 5). У мужчин после приема препарата медиана концентрации витамина D3 составила 65,32 нг/мл, повышение в 2,42 раза (Рисунок 6).
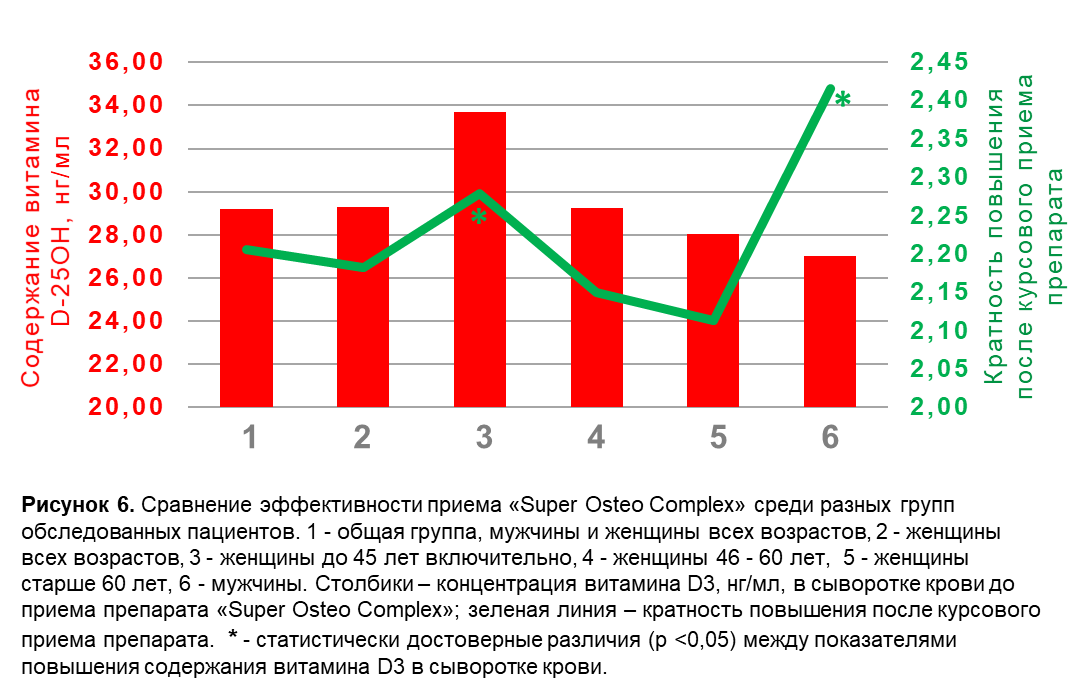
4.4. Кратность повышения концентрации витамина D3 в различных группах
Эффективность приема мицеллярного препарата витамина D3 различалась в разных группах обследованных пациентов. Значения повышения концентрации витамина D3 после окончания курсового приема в группе женщин до 45 лет и в группе мужчин были значительно выше (р<0,05), чем в группах женщин от 46 до 60 лет и старше 60 лет. Это говорит о наибольшей эффективности препарата «Super Osteo Complex» в двух группах - (1) в группе мужчин и (2) в группе женщин младшей возрастной группы (до 45 лет включительно).
5. Обсуждение результатов
Проведенное исследование базировались на общепринятой методике определения концентрации витамина D3 в сыворотке крови. Выбранная доза для перорального применения тоже не была уникальной, ранее дозы холекальциферола такого же порядка использовались для коррекции гиповитаминозов D3 [13]. Существенным отличием проведенного исследования было применение мицеллярной формы витамина D3, которая фантастически повышала его биодоступность. В естественных условиях процесс усвоения витамина D3 в кишечнике реализуется исключительно после формирования D3-содержащих мицелл, которые образуются в результате взаимодействия гидрофобного D3 с (1) липидами, поступающими с пищей и частично гидролизованными под воздействием липаз, и (2) компонентами желчи, которые обладают свойствами поверхностно-активных веществ (детергентов). Поэтому при нарушении мицеллообразования в результате болезней желудочно-кишечного тракта или вследствие физиологических причин (старение) происходит нарушение всасывания витамина D3. Искусственная инкорпорация витамина D3 в мицеллы в виде готовых лекарств или биологически-активных добавок позволяет улучшить усвоение витамина D3 в кишечнике и нейтрализовать негативные эффекты гиповитаминоза D3 при патологии или старении.
Главным результатом исследования стало доказательство того, что мицеллярный препарат «Super Osteo Complex» повышал содержание витамина D3 в крови в среднем в 2,1 - 2,4 раза. Исключений не было. Следует признать, что применение масляных немицеллярных форм витамина D3 тоже приводило к повышению его концентрации в крови в 2-3 раза, но это повышение достигалось после приема препарата в течение 150 дней [14]. При применении мицеллярного препарата «Super Osteo Complex» такой же эффект был получен после 25 - 60 дней приема. Исследование эффективности аналогичного мицеллярного препарата D3 «LipoMicel® Vitamin D», проведенное австралийско-канадским научным коллективом, также показало более высокую эффективность мицеллярных форм [15]. В этой работе было зарегистрировано 7-кратное повышение содержания витамина D3 после приема мицеллярного препарата в течение 30 дней. Повышение D3 в результате приема препарата «LipoMicel® Vitamin D» была не просто большим, оно было чрезмерным, так как могло привести к развитию гипервитаминоза, что негативно характеризует «LipoMicel® Vitamin D».
6. Заключение
Настоящее исследование доказало, что мицеллярный препарат «Super Osteo Complex» (ООО «Мицеллайн») является высоко эффективным инструментом для быстрого повышения содержания витамина D3 (холекальциферол) в сыворотке крови женщин и мужчин различных возрастов. Достижение положительного эффекта от приема препарата «Super Osteo Complex» занимало в 2,5 - 6 раз меньше времени, чем от применения традиционных масляных растворов витамина D3. Нежелательных побочных эффектов не наблюдалось.
7. Список литературы:
1. Holick M. F. Vitamin D deficiency. New England journal of medicine. 2007; Vol. 357(3): 266-281. https://doi.org/10.1056/NEJMra070553
2. Aranow C. Vitamin D and the immune system. Journal of investigative medicine. 2011; Vol. 59(6): 881-886. https://doi.org/10.2310/jim.0b013e31821b8755
3. da Silva A. A. et al. Endogenous melanocortin system activity contributes to the elevated arterial pressure in spontaneously hypertensive rats. Hypertension. 2008; Vol. 51(4): 884-890. https://doi.org/10.1161/HYPERTENSIONAHA.107.100636
4. Anglin R.E.S. et al. Vitamin D deficiency and depression in adults: systematic review and meta-analysis. The British journal of psychiatry. 2013; Vol. 202(2): 100-107. https://doi.org/10.1192/bjp.bp.111.106666
5. MacLaughlin J. et al. Aging decreases the capacity of human skin to produce vitamin D3. The Journal of clinical investigation. 1985; Vol. 76(4): 1536-1538. https://doi.org/10.1172/JCI112134
6. Weinsier R.L., Krumdieck C.L. Dairy foods and bone health: examination of the evidence. The American Journal of Clinical Nutrition. 2000; Vol. 72(3): 681-689. https://doi.org/10.1093/ajcn/72.3.681
7. Bischoff-Ferrari H.A. et al. A pooled analysis of vitamin D dose requirements for fracture prevention. New England Journal of Medicine. 2012; Vol. 367(1): 40-49. https://doi.org/10.1056/NEJMoa1109617
8. Dawson-Hughes B. et al. Dietary fat increases vitamin D-3 absorption. Journal of the Academy of Nutrition and Dietetics. 2015; Vol. 115(2): 225-230. https://doi.org/10.1016/j.jand.2014.09.014
9. Wortsman J. et al. Decreased bioavailability of vitamin D in obesity. The American journal of clinical nutrition. 2000; Vol. 72(3): 690-693. https://doi.org/10.1093/ajcn/72.3.690
10. Arden N.K. et al. Persistence with teriparatide in patients with osteoporosis: the UK experience. Osteoporosis International. 2006; Vol. 17: 1626-1629. https://doi.org/10.1007/s00198-006-0171-5
11. Bikle D.D. Vitamin D metabolism, mechanism of action, and clinical applications. Chemistry & Biology. 2014; Vol. 21(3): 319-329. https://doi.org/10.1016/j.chembiol.2013.12.016
12. Клинические рекомендации. Дефицит витамина D у взрослых: диагностика, лечение и профилактика. Российская ассоциация эндокринологов, Москва, 2015
13. Trivedi D.P. et al. Effect of four monthly oral vitamin D3 (cholecalciferol) supplementation on fractures and mortality in men and women living in the community: randomized double blind controlled trial. British Medical Journal. 2003; 326: 469–474.
14. Yahyavi S.K. et al. Influence of cholecalciferol supplementation on changes in total 25OHD, free 25OHD, and free 25OHD% in relation to calcium, bone, and glucose homeostasis in young, infertile men. The Journal of steroid biochemistry and molecular biology. 2025; Vol. 246: 106640. https://doi.org/10.1016/j.jsbmb.2024.106640
15. Solnier J. et al. A Comparison and Safety Evaluation of Micellar versus Standard Vitamin D3 Oral Supplementation in a Randomized, Double-Blind Human Pilot Study. Nutrients. 2024; Vol. 16(11): 1573. https://doi.org/10.3390/nu16111573
Автор: Чеботарь И.В. - доктор медицинских наук (03.02.03 – микробиология), заведующий лабораторией молекулярной микробиологии Федерального государственного автономного образовательного учреждения высшего образования «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Министерства здравоохранения Российской Федерации (ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, Москва)